Acids Bases And Salts Notes PDF Download: हमारे दैनिक जीवन में उपयोग होने वाली अनेक वस्तुएँ जैसे नींबू, सिरका, साबुन, बेकिंग सोडा, दवाइयाँ और टूथपेस्ट—इन सभी में कहीं-न-कहीं अम्ल, क्षारक एवं लवण पाए जाते हैं। भोजन का खट्टा या कड़वा स्वाद, पेट की अम्लता, दाँतों का क्षय, कपड़े धोने का सोडा, यहाँ तक कि टूटी हुई हड्डियों पर लगाया जाने वाला प्लास्टर—इन सबका संबंध इसी अध्याय से है।
NCERT कक्षा 10 विज्ञान का अध्याय 2 “अम्ल, क्षारक एवं लवण” विद्यार्थियों के लिए अत्यंत महत्वपूर्ण अध्याय है, क्योंकि इसमें न केवल रासायनिक अभिक्रियाएँ, pH स्केल, सूचक (Indicators) जैसे सिद्धांत समझाए गए हैं, बल्कि उनके दैनिक जीवन में उपयोग को भी सरल उदाहरणों के साथ बताया गया है। यह अध्याय बोर्ड परीक्षाओं में अक्सर लॉन्ग आंसर, न्यूमेरिकल, अभिक्रिया और कारण बताइए जैसे प्रश्नों के रूप में पूछा जाता है।
इस पोस्ट में आपको अम्ल, क्षारक एवं लवण के Handwritten Style Notes सरल और व्यवस्थित रूप में मिलेंगे, ताकि विद्यार्थी इन्हें आसानी से समझ सकें, याद कर सकें और परीक्षा में सीधे लिख सकें। ये नोट्स NCERT पाठ्यपुस्तक पर आधारित, परीक्षा-उपयोगी और पूरी तरह स्टूडेंट-फ्रेंडली हैं।
अम्ल (Acids)
🔹 परिभाषा
वे पदार्थ जो जलीय विलयन में H⁺ या H₃O⁺ आयन उत्पन्न करते हैं, अम्ल कहलाते हैं।
🔹 अम्लों के गुण
- स्वाद: खट्टा
- नीले लिटमस को लाल करते हैं
- विद्युत का चालन करते हैं (केवल जलीय विलयन में)
- धातु से अभिक्रिया कर हाइड्रोजन गैस निकालते हैं
🔹 सामान्य अम्ल
| अम्ल | रासायनिक सूत्र |
|---|---|
| हाइड्रोक्लोरिक अम्ल | HCl |
| सल्फ्यूरिक अम्ल | H₂SO₄ |
| नाइट्रिक अम्ल | HNO₃ |
| एसीटिक अम्ल | CH₃COOH |
| अम्ल वे रासायनिक पदार्थ होते हैं जो जल में घुलने पर हाइड्रोजन आयन (H⁺) अथवा हाइड्रोनियम आयन (H₃O⁺) उत्पन्न करते हैं। अम्लों का स्वाद सामान्यतः खट्टा होता है। उदाहरण के लिए नींबू, सिरका, इमली आदि खट्टे होते हैं क्योंकि इनमें विभिन्न प्रकार के अम्ल पाए जाते हैं। अम्लों की सबसे महत्वपूर्ण विशेषता यह है कि वे नीले लिटमस पत्र को लाल कर देते हैं। अम्ल केवल जलीय विलयन में ही अपने अम्लीय गुण प्रदर्शित करते हैं, क्योंकि जल की उपस्थिति में ही H⁺ आयन उत्पन्न होते हैं। सूखी अवस्था में अम्ल अम्लीय व्यवहार नहीं दिखाते। सामान्य अम्लों में हाइड्रोक्लोरिक अम्ल (HCl), सल्फ्यूरिक अम्ल (H₂SO₄), नाइट्रिक अम्ल (HNO₃) और एसीटिक अम्ल (CH₃COOH) प्रमुख हैं। ये अम्ल प्रयोगशालाओं, उद्योगों और दैनिक जीवन में व्यापक रूप से उपयोग किए जाते हैं। |

2️⃣ क्षारक (Bases) एवं क्षार (Alkali)
🔹 परिभाषा
वे पदार्थ जो जलीय विलयन में OH⁻ आयन उत्पन्न करते हैं।
🔹 क्षार (Alkali)
जो क्षारक जल में घुलनशील होते हैं, उन्हें क्षार कहते हैं।
🔹 गुण
- स्वाद: कड़वा
- लाल लिटमस को नीला करते हैं
- फिनॉल्फ्थेलिन को गुलाबी बनाते हैं
🔹 उदाहरण
| क्षारक | सूत्र |
|---|---|
| सोडियम हाइड्रॉक्साइड | NaOH |
| पोटैशियम हाइड्रॉक्साइड | KOH |
| कैल्सियम हाइड्रॉक्साइड | Ca(OH)₂ |
| क्षारक वे पदार्थ होते हैं जो जल में घुलकर हाइड्रॉक्साइड आयन (OH⁻) उत्पन्न करते हैं। क्षारकों का स्वाद सामान्यतः कड़वा होता है और उनका स्पर्श साबुन जैसा लगता है। क्षारक लाल लिटमस पत्र को नीला कर देते हैं। जो क्षारक जल में पूरी तरह घुल जाते हैं, उन्हें क्षार (Alkali) कहा जाता है। जैसे – सोडियम हाइड्रॉक्साइड (NaOH) और पोटैशियम हाइड्रॉक्साइड (KOH) क्षार हैं क्योंकि ये जल में आसानी से घुल जाते हैं। क्षारक रासायनिक रूप से संक्षारक (corrosive) होते हैं, इसलिए इन्हें छूना या चखना हानिकारक हो सकता है। प्रयोगशाला में इनका उपयोग अत्यंत सावधानी से किया जाता है। |

3️⃣ सूचक (Indicators)
🔹 प्राकृतिक सूचक
- लिटमस
- हल्दी
- लाल पत्ता गोभी
🔹 कृत्रिम सूचक
| सूचक | अम्ल में | क्षार में |
|---|---|---|
| लिटमस | लाल | नीला |
| फिनॉल्फ्थेलिन | रंगहीन | गुलाबी |
| मिथाइल ऑरेंज | लाल | पीला |
| सूचक वे पदार्थ होते हैं जो किसी विलयन की अम्लीय या क्षारीय प्रकृति को रंग परिवर्तन द्वारा बताते हैं। सूचक दो प्रकार के होते हैं – प्राकृतिक और कृत्रिम। प्राकृतिक सूचक: प्राकृतिक सूचकों में लिटमस, हल्दी और लाल पत्ता गोभी शामिल हैं। लिटमस एक प्राकृतिक सूचक है जो लिचेन नामक पौधे से प्राप्त होता है। कृत्रिम सूचक: कृत्रिम सूचकों में फिनॉल्फ्थेलिन और मिथाइल ऑरेंज प्रमुख हैं। फिनॉल्फ्थेलिन अम्लीय माध्यम में रंगहीन और क्षारीय माध्यम में गुलाबी हो जाता है, जबकि मिथाइल ऑरेंज अम्ल में लाल और क्षार में पीला रंग दिखाता है। |

4️⃣ अम्लों की प्रमुख अभिक्रियाएँ
(A) धातु के साथ
अम्ल + धातु → लवण + H₂↑
| जब अम्ल किसी धातु के साथ अभिक्रिया करता है, तो हाइड्रोजन गैस निकलती है और एक लवण बनता है। यह अभिक्रिया इस तथ्य को दर्शाती है कि अम्लों में हाइड्रोजन उपस्थित होता है। |
उदाहरण:
Zn + 2HCl → ZnCl₂ + H₂
| इस अभिक्रिया में जिंक धातु हाइड्रोक्लोरिक अम्ल से अभिक्रिया करके जिंक क्लोराइड और हाइड्रोजन गैस उत्पन्न करती है। हाइड्रोजन गैस की पहचान जलती हुई तीली पास लाने पर “पॉप” ध्वनि से की जाती है। |
(B) धातु कार्बोनेट के साथ
अम्ल + धातु कार्बोनेट → लवण + CO₂ + H₂O
| जब कोई अम्ल किसी धातु कार्बोनेट या धातु हाइड्रोजन कार्बोनेट के साथ अभिक्रिया करता है, तो इस अभिक्रिया के परिणामस्वरूप लवण, जल तथा कार्बन डाइऑक्साइड गैस (CO₂) उत्पन्न होती है। यह अम्लों की एक अत्यंत महत्वपूर्ण और विशिष्ट अभिक्रिया है, जिसे प्रयोगशाला में आसानी से प्रदर्शित किया जा सकता है। |
Na₂CO₃ + 2HCl → 2NaCl + H₂O + CO₂
| जब सोडियम कार्बोनेट (Na₂CO₃) में हाइड्रोक्लोरिक अम्ल (HCl) मिलाया जाता है, तो तीव्र बुलबुले निकलते हैं, जो कार्बन डाइऑक्साइड गैस के कारण होते हैं। |
5️⃣ उदासीनीकरण अभिक्रिया (Neutralization)
अम्ल + क्षार → लवण + जल
HCl + NaOH → NaCl + H₂O
| जब कोई अम्ल किसी क्षार के साथ अभिक्रिया करता है, तो दोनों के प्रभाव एक-दूसरे को समाप्त कर देते हैं। इस अभिक्रिया को उदासीनीकरण अभिक्रिया कहा जाता है। इस अभिक्रिया के परिणामस्वरूप लवण और जल बनते हैं। यह अभिक्रिया दैनिक जीवन में अत्यंत महत्वपूर्ण है, जैसे पेट की अम्लता को कम करने के लिए एंटासिड का उपयोग किया जाता है। |
👉 यह बहुत महत्वपूर्ण परीक्षा प्रश्न है।
6️⃣ जलीय विलयन का महत्व
- सूखा HCl गैस अम्लीय नहीं होता
- अम्लीय गुण केवल जल की उपस्थिति में आते हैं
HCl + H₂O → H₃O⁺ + Cl⁻
| अम्ल केवल जलीय विलयन में ही अम्लीय गुण प्रदर्शित करते हैं। जल की अनुपस्थिति में H⁺ आयन उत्पन्न नहीं हो पाते। |
👉 H⁺ आयन अकेले नहीं रहते, हमेशा H₃O⁺ बनाते हैं
7️⃣ pH स्केल (अत्यंत महत्वपूर्ण)
| pH मान | प्रकृति |
|---|---|
| 0–6 | अम्लीय |
| 7 | उदासीन |
| 8–14 | क्षारीय |
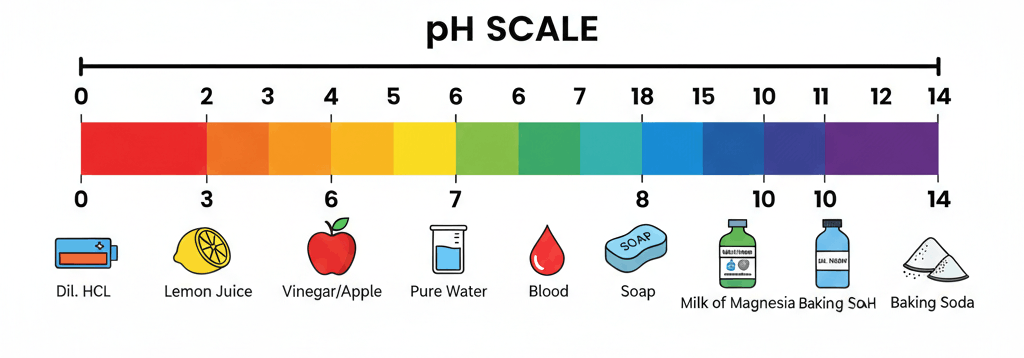
| pH स्केल का उपयोग किसी विलयन की अम्लीय या क्षारीय शक्ति मापने के लिए किया जाता है। pH स्केल का मान 0 से 14 तक होता है। pH = 7 → उदासीन विलयन pH < 7 → अम्लीय विलयन pH > 7 → क्षारीय विलयन pH मान जितना कम होगा, अम्ल उतना ही अधिक प्रबल होगा। pH मान जितना अधिक होगा, क्षार उतना ही अधिक प्रबल होगा। |
🔹 महत्वपूर्ण तथ्य
- pH कम ⇒ अम्ल अधिक प्रबल
- pH अधिक ⇒ क्षार अधिक प्रबल
8️⃣ दैनिक जीवन में pH का महत्व
🔹 पेट में अम्लता
- HCl अधिक बनने पर दर्द
- एंटासिड (Mg(OH)₂) उपयोगी
| pH हमारे दैनिक जीवन में अत्यंत महत्वपूर्ण भूमिका निभाता है। हमारे पेट में हाइड्रोक्लोरिक अम्ल पाया जाता है, जो भोजन के पाचन में सहायता करता है। अधिक अम्ल बनने पर पेट में जलन और दर्द होता है, जिसे एंटासिड द्वारा नियंत्रित किया जाता है। |
🔹 दाँतों का क्षय
- pH < 5.5 होने पर इनैमल नष्ट
- क्षारीय टूथपेस्ट उपयोगी
| दाँतों के क्षय का मुख्य कारण मुँह का pH 5.5 से कम होना है। भोजन के बाद बैक्टीरिया अम्ल बनाते हैं, जिससे दाँतों का इनैमल नष्ट हो सकता है। |
🔹 मधुमक्खी का डंक
- अम्लीय → बेकिंग सोडा से राहत
| मधुमक्खी के डंक में अम्ल पाया जाता है, इसलिए उस स्थान पर बेकिंग सोडा जैसे क्षारक का उपयोग करने से राहत मिलती है। |
9️⃣ लवण (Salts)
🔹 परिभाषा
अम्ल और क्षार की अभिक्रिया से बने यौगिक।
🔹 लवण का pH
| अम्ल | क्षार | लवण की प्रकृति |
|---|---|---|
| प्रबल | प्रबल | उदासीन |
| प्रबल | दुर्बल | अम्लीय |
| दुर्बल | प्रबल | क्षारीय |
| लवण वे यौगिक होते हैं जो अम्ल और क्षार की अभिक्रिया से बनते हैं। लवण अम्लीय, क्षारीय या उदासीन हो सकते हैं, यह इस बात पर निर्भर करता है कि वे किस अम्ल और किस क्षार से बने हैं। उदाहरण: सोडियम क्लोराइड (NaCl) एक उदासीन लवण है। |

🔟 साधारण नमक से प्राप्त रसायन (VERY IMPORTANT)
🔹 (A) सोडियम हाइड्रॉक्साइड – क्लोर-क्षार प्रक्रिया
2NaCl + 2H₂O → 2NaOH + Cl₂ + H₂
🔹 (B) बेकिंग सोडा (NaHCO₃)
- एंटासिड
- केक/पकौड़े फुलाने में
🔹 (C) वॉशिंग सोडा (Na₂CO₃·10H₂O)
- कपड़े धोने
- कठोर जल को मुलायम करने में
| सोडियम क्लोराइड से अनेक महत्वपूर्ण रसायन बनाए जाते हैं। क्लोर-क्षार प्रक्रिया द्वारा सोडियम हाइड्रॉक्साइड, क्लोरीन और हाइड्रोजन प्राप्त होते हैं। बेकिंग सोडा का उपयोग केक-पकौड़े फुलाने, एंटासिड और अग्निशामक में किया जाता है। वॉशिंग सोडा का उपयोग कपड़े धोने, काँच उद्योग और जल की कठोरता दूर करने में होता है। |
1️⃣1️⃣ क्रिस्टलन का जल (Water of Crystallization)
| यौगिक | सूत्र |
|---|---|
| कॉपर सल्फेट | CuSO₄·5H₂O |
| वॉशिंग सोडा | Na₂CO₃·10H₂O |
| कुछ लवणों के क्रिस्टलों में निश्चित मात्रा में जल जुड़ा रहता है, जिसे क्रिस्टलन का जल कहते हैं। जैसे – कॉपर सल्फेट (CuSO₄·5H₂O)। गर्म करने पर यह जल निकल जाता है और रंग बदल जाता है। |
1️⃣2️⃣ प्लास्टर ऑफ पेरिस (PoP)
CaSO₄·2H₂O → CaSO₄·½H₂O + 1½H₂O
उपयोग
- टूटी हड्डियाँ
- खिलौने
- सजावट
| प्लास्टर ऑफ पेरिस जिप्सम को गर्म करने से प्राप्त किया जाता है। यह सफेद चूर्ण होता है जो जल मिलाने पर कठोर हो जाता है। इसका उपयोग टूटी हड्डियाँ जोड़ने, खिलौने और सजावट की वस्तुएँ बनाने में किया जाता है। |
All Chapter Notes Links
| Chapter-1 : Chemical Reactions & Equations / अध्याय-1 : रासायनिक अभिक्रियाएँ एवं समीकरण | English Medium | Hindi Medium |
